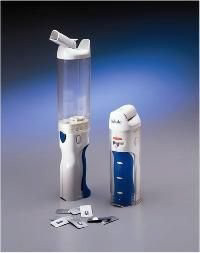
(AUNO/ Ciencia) La insulina inhalable, cuyo lanzamiento en la Argentina había generado expectativas en los pacientes con diabetes, no llegará finalmente al país ya que ha sido discontinuada por el laboratorio farmacéutico que la producía, la multinacional Pfizer.
El producto, que había sido lanzado en junio en Europa y un mes después en los Estados Unidos, “no tuvo aceptación entre los pacientes y tampoco en la comunidad médica”, que prefirieron continuar con los métodos tradicionales de aplicación de la insulina inyectable.
Pfizer anunció a mediados de octubre la retirada general de la primera insulina inhalada, ya que, según la compañía, el producto, que se comercializaba bajo la marca Exubera, no alcanzó las ventas esperadas.
La decisión da por tierra con la expectativa que había generado entre los pacientes el anuncio del laboratorio, realizado hace más de dos años, del lanzamiento de un nuevo producto que reemplazaba a las inyecciones.
Los motivos para la retirada han sido estrictamente económicos, ya que se trata de un medicamento “seguro y eficaz”, según puntualizó en un comunicado la dirección médica del laboratorio Pfizer.
El fracaso comercial del producto en los países en los que había sido lanzado obedeció, en principio, a la falta de cobertura por parte de la seguridad social, ya que se trata de un producto cuyo costo, en promedio, triplica al de la insulina tradicional.
Además, se estima que los pacientes no terminaron de aceptarlo ya que el sistema de medición de las dosis era diferente al de la insulina inyectable: “La administración no permitía ajustar con precisión la cantidad de insulina necesaria, ya que un miligramo equivalía a tres unidades de las de antes”, comentó el integrante de una asociación de pacientes al diario El País de Madrid.
El nuevo producto había aparecido como una esperanza para aquellos pacientes con diabetes tipo 2 que deben inyectarse la medicación entre dos y tres veces por día, especialmente aquellos que padecen aversión a los pinchazos, lo que deriva en frecuentes abandonos del tratamiento.
La insulina inhalable consiste en un polvo que se administra a través de un dispositivo similar a los que se usan para la medicación broncodilatadora.
Según los estudios clínicos realizados, el producto es tan eficaz como las insulinas rápidas que se inyectan y los únicos efectos adversos que se habían observado eran tos, sensación de falta de aire y sequedad en la boca. La Administración de Alimentos y Medicamentos (FDA) de los Estados Unidos, había desaconsejado su uso en personas con problemas respiratorios.
EV